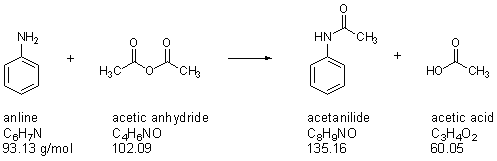
استانیلید نوعی آمید است. روش های متنوعی برای سنتز استانیلید وجود دارد. برخی از این روش ها در واکنش های زیر آورده شده است:
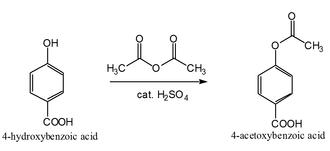
روش اول: آسیلاسیون آنیلین با انیدرید استیک:
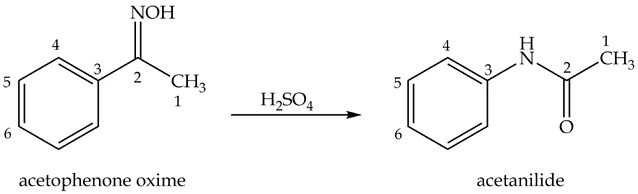
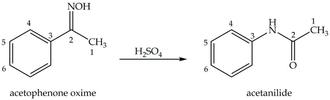
روش دوم: نوآرایی بکمن بر روی اکسیم ها:
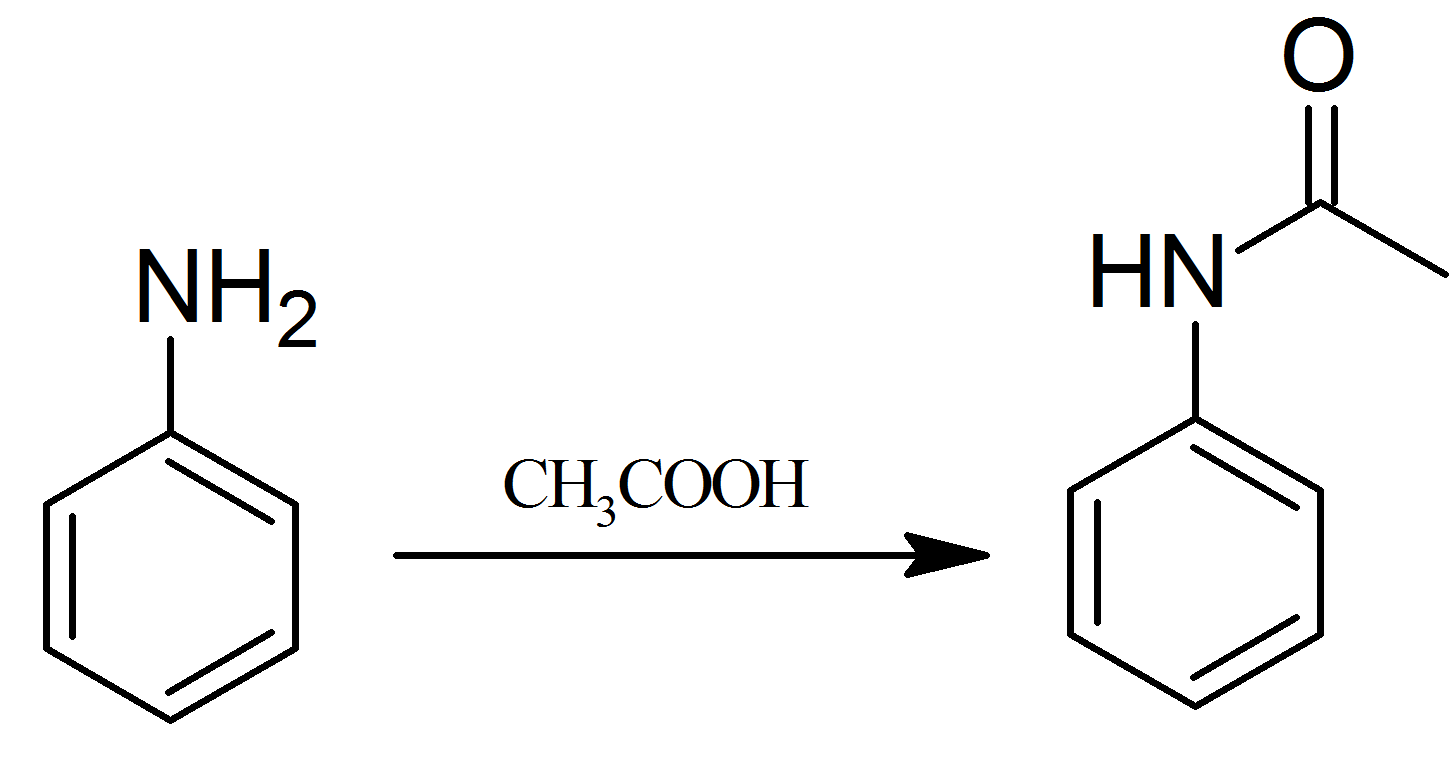
روش سوم: آسیلاسیون آنیلین با استیک اسید:
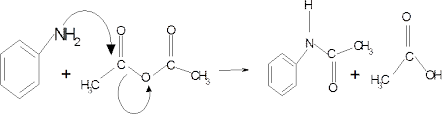
مکانیسم آسیلاسیون با انیدرید استیک به صورت زیر می باشد. در این واکنش جفت الکترون های روی نیتروژن آمینی به کربن کربونیل حمله می کنند و پیوند با اکسیژن کناری را قطع می کنند. بنابراین استانیلید و یک مولکول اسید استیک به وجود می آید:
واکنش های مشابهی نیز در تهیه آسپیرین، استامینوفن و ... وجود دارد:
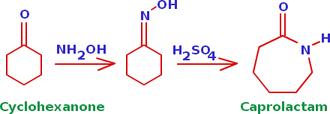
نوآرایی بکمن (Beckmann Rearrangement)
در کنار این آزمایش، آزمایش دیگری هست موسوم به نوآرایی بکمن که مطالعه آن به همراه آزمایش استانیلید ضروریست.
نوآرایی بکمن نوعی واکنش است که در آن یک اکسیم (یعنی
ترکیبی که در آن یک کربن با باند دوگانه به NOH- وصل شده است.) در حضور
اسید به یک آمید تبدیل می شود.
راه حل نوشتن محصول واکنش نوآرایی بکمن:
به کربن
حامل باند دوگانه نیتروژن توجه کنید. این کربن قرار است بشود کربونیل. هر
استخلافی هم به آن وصل است، کنار آن می ماند. حالا نیتروژن می افتد پشت
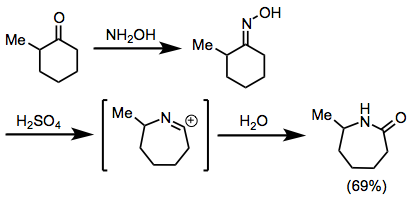
کربن کربونیل. به مثال زیر توجه کنید. کربن شماره 2 به کربونیل تبدیل شده و
متیلی که به آن وصل بود نیز به کربونیل وصل شده است. نیتروژن نیز می افتد
بین کربونیل و حلقه. به عبارت دیگر، کربن اکسیم (شماره 2) همزمان به یک
متیل (کربن 1) و حلقه وصل است. حالا کربن 2 شده کربونیل. ممکن است سؤالی
پیش بیاید و آن این که نیتروژن به حلقه وصل می شود یا متیل؟ جواب این است
که همیشه حلقه آروماتیک نسبت به متیل، اتیل و سایر آلکیل ها برای در اختیار
گرفتن نیتروژن اولویت دارد.
در مثال های زیر آمیدهای حلقوی (لاکتام) به وجود آمده اند: